Dystrophie musculaire : du nouveau en thérapie cellulaire

Photo : UdeS
Une équipe de recherche conjointe entre l’Université de Sherbrooke et le Nestlé Institute of Health Sciences a développé un protocole pour la génération in vitro de cellules souches musculaires squelettiques avec une rapidité et une efficacité sans précédent. Grâce à cette nouvelle méthode, il est maintenant possible de greffer des cellules souches avec succès à même un muscle atteint de dystrophie musculaire. Cette approche ouvre la porte à une potentielle nouvelle façon de traiter cette maladie dégénérative.
Combattre la maladie une cellule à la fois
Les personnes atteintes de dystrophie musculaire sont grandement limitées dans leurs activités. La maladie génétique provoque une dégénérescence progressive des fibres musculaires, et dans certaines formes de cette condition, elle peut entraîner une perte complète d’autonomie. Il n’y a pas de traitement efficace offert aux personnes souffrant de la maladie, ne permettant actuellement qu’à améliorer, autant que possible, l’autonomie et la qualité de vie des personnes atteintes.
Le professeur Florian Bentzinger, titulaire de la Chaire CRMUS sur la médecine régénérative du muscle squelettique, et son équipe s’intéressent depuis de nombreuses années à la régénération cellulaire – aux cellules souches – dans les cas de dystrophie musculaire.
La capacité des cellules souches musculaires saines à ajouter leur matériel génétique à des fibres musculaires malades fait de ces cellules des candidates très intéressantes pour le traitement de la dystrophie musculaire. En introduisant du matériel génétique sain dans les fibres du receveur défaillant, il pourrait être possible de ralentir ou de guérir la maladie.
Cependant, il est très difficile d'obtenir des quantités suffisantes de cellules souches musculaires qui ont la capacité de se greffer dans un muscle malade. À ce jour, les protocoles de production de cellules souches musculaires squelettiques telles qu’utilisées par l’équipe du Pr Bentzinger, les cellules souches pluripotentes induites (CSPi), demandent beaucoup de temps (3 à 5 semaines ou plus), génèrent des cultures impures, et sont conçus pour des cellules adhérentes, ce qui, pour une production à grande échelle, nécessite une énorme quantité d'articles de culture cellulaire en plastique.
Le nouveau protocole du Pr Bentzinger et de ses collaborateurs renverse la vapeur en permettant désormais de produire des cellules souches musculaires squelettiques à partir de cellules humaines CSPi avec une pureté de 99 %, en seulement deux semaines. De plus, le protocole est conçu pour être réalisé en suspension, ce qui permet une production à grande échelle facile à mettre en œuvre. Une découverte très prometteuse!
Cellules CSPi comme source de progéniteurs musculaires
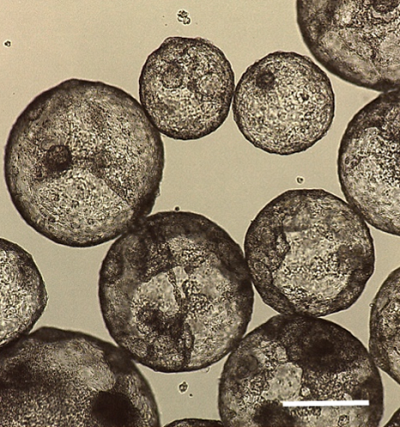
L'image montre des agrégats 3D en suspension (également appelés embryoïdes) de cellules souches pluripotentes induites et de cellules auxiliaires. Les cellules auxiliaires de ces agrégats 3D favorisent la génération de cellules souches musculaires à partir des cellules CSPi. Chacun de ces agrégats est composé de centaines de milliers de cellules.
Photo : Fournie
Les cellules souches CSPi utilisées par l’équipe de Pr Bentzinger ont certaines particularités qui les rendent très spéciales :
- Elles peuvent donner naissance à des cellules qui auront les mêmes caractéristiques qu’elles, et ce, même après un grand nombre de divisions cellulaires.
- Elles ne sont pas encore spécialisées, c’est-à-dire qu’elles ont le potentiel de se transformer en presque n’importe quelles cellules du corps.
Une greffe de cellules souches réussie
La transplantation des cellules souches musculaires, dérivées de cellules CSPi, utilisant ce nouveau protocole, a montré une grande efficacité dans des modèles précliniques de la dystrophie musculaire : les muscles deviennent plus forts et plus sains.
Les cellules souches saines transplantées dans les muscles dystrophiques, marquées en rouge dans la figure, se multiplient efficacement et se fusionnent aux fibres musculaires porteuses du gène responsable de la maladie. Lorsqu’elles fusionnent avec les tissus musculaires, les cellules saines ajoutent leur noyau à la fibre musculaire défaillante pour favoriser la guérison. Elles se complètent. La cohabitation des deux cellules et leur fusion au tissu musculaire permettent au tissu d’amorcer sa régénération.
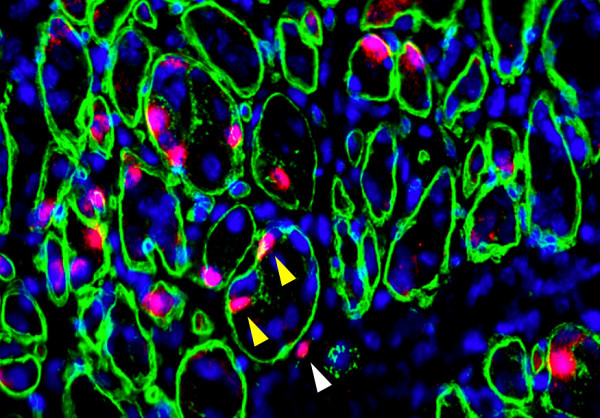
Photo : Fournie
Ce qui est intéressant à constater, c’est que plusieurs cellules souches n'ont pas fusionné directement avec les fibres musculaires hôtes. Certaines ont pu se réactiver et se diviser dans le tissu malade pour générer davantage de cellules souches. Ainsi, le traitement avec ces cellules pourrait potentiellement avoir un effet à vie.
Protocole de création
Pour que la greffe soit efficace, les cellules souches greffées sont générées à l'aide de deux autres types de cellules en agrégats 3D. Cela comprend un type de cellule produisant de grandes quantités de tissu conjonctif et un type de cellule que l'on trouve généralement dans les vaisseaux sanguins. Ensemble, elles soutiennent la génération de cellules souches musculaires à partir des cellules CSPi. L’équipe du Pr Bentzinger et du Nestlé Institute of Health Sciences ont développé le protocole pour que les agrégats puissent se former dans un environnement liquide. Cela comporte plusieurs avantages, tels que la création de cellules souches pures, la facilité de reproduction et la production d’un bon nombre d’agrégats dans un espace restreint.
Cela est très prometteur pour le traitement cellulaire, car cela ouvre la voie à, entre autres, la simulation de la maladie à même la solution.
À propos du Pr Florian Bentzinger
Titulaire de la Chaire CRMUS sur la médecine régénérative du muscle squelettique
Professeur au Département de pharmacologie-physiologie, FMSS
Membre de l’Institut de pharmacologie de Sherbrooke
Chercheur au CRCHUS