Comment nos cellules protègent leur ADN… et ce que la levure nous apprend sur le vieillissement

Photo : Mathieu Lanthier - UdeS
Pourquoi nos cellules vieillissent-elles ? Une partie de la réponse se cache tout au bout de nos chromosomes, là où se trouvent les télomères. Ces petites structures agissent comme des capuchons protecteurs : elles empêchent notre ADN de s'abîmer lorsque les cellules se divisent. Mais à chaque division, les télomères raccourcissent un peu. Lorsqu'ils deviennent trop courts, la cellule perd sa capacité à fonctionner correctement, ce qui est lié au vieillissement et à plusieurs maladies, dont certains cancers.
Pour ralentir ce processus, les cellules disposent d'un outil crucial : la télomérase. Cette enzyme a pour rôle de réparer et de rallonger les télomères, contribuant ainsi à maintenir la santé des cellules. Mieux comprendre son fonctionnement est donc un enjeu majeur pour la recherche sur le vieillissement.
Dans une étude publiée dans la revue Science, Cryo–electron microscopy structure of the budding yeast telomerase holoenzyme une équipe internationale de chercheurs composée de Raymund Wellinger, professeur-chercheur à la FMSS de l'Université de Sherbrooke, Pascal Chartrand, professeur à l'Université de Montréal et Thi Hoang Duong Nguyen, du Laboratory of Molecular Biology a réussi un exploit : identifier pour la première fois la structure atomique de la télomérase de la levure. Si cet organisme peut sembler éloigné de l'humain, il est pourtant un modèle de choix en biologie, car de nombreux mécanismes fondamentaux y sont semblables aux nôtres.
Cette publication présente un travail colossal de qualité exceptionnelle, remarquée aussi par un des arbitres qui commente "je ne pensais pas voir cette découverte de mon vivant" !
Pr Raymund Wellinger professeur-chercheur à la FMSS
Grâce à une technologie d'imagerie de pointe, l'équipe de chercheurs a découvert que la télomérase de la levure a une structure architecturale très complexe. En son centre se trouve un long morceau d'ARN qui agit comme un échafaudage, maintenant ensemble de nombreuses protéines. Certaines font partie du noyau central très stable, essentiel à l'activité de l'enzyme, tandis que d'autres sont attachées de manière plus souple, ce qui donne à l'ensemble une grande flexibilité.
Au-delà des découvertes autour du rôle de l'ARN, les résultats de l'étude mettent en évidence que la protéine Est3, un petit factor spécifique à la télomérase et méconnue jusqu'ici, joue un rôle central en tant que plateforme d'interactions protéines–protéines, stabilisant l'ensemble de la télomérase. La perturbation des interactions d'Est3 avec d'autres facteurs comme Est2 et Pop1 entraîne un raccourcissement des télomères et un vieillissement accéléré des cellules, démontrant l'importance fonctionnelle de ces contacts. La structure confirme également qu'Est3 est un homologue structural d'une protéine télomérique humaine faisant partie des télomères.
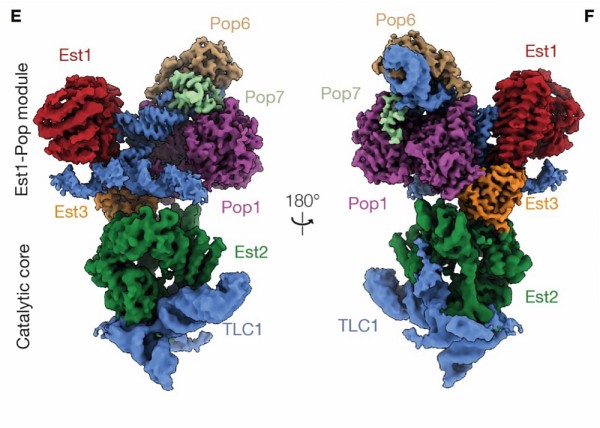
Finalement, un sous-complexe de trois protéines appelées Pop1/6/7 et qui est partagé avec des enzymes de maturation des ARN, facilite l'association de trois protéines essentielles pour les fonctions de la télomérase via des interactions combinées ARN–protéine. De façon remarquable, l'équipe de chercheurs a identifié une boucle spécifique de Pop1 nécessaire au maintien des télomères, mais dispensable pour la maturation des ARN, démontrant que Pop1 est une véritable sous-unité de la télomérase dotée d'une fonction spécifique aux télomères.
Au-delà de la levure, ces résultats permettent de mieux comprendre comment la télomérase s'assemble et fonctionne, même lorsqu'elle repose sur un long ARN souple et complexe. Ces principes mis au jour pourraient s'appliquer à la télomérase d'autres espèces, mais aussi à d'autres structures cellulaires contenant de longues molécules d'ARN. L'étude montre enfin comment, au fil de l'évolution, différentes formes d'organisation ont émergé selon les espèces, tout en conservant une fonction essentielle : protéger l'ADN et assurer le bon fonctionnement des cellules, un enjeu central du vieillissement et des maladies qui y sont associées.
À propos du Pr Wellinger
Raymund Wellinger est professeur associé à la Faculté de médecine et des sciences de la santé de l'Université de Sherbrooke et chercheur au Centre de recherche sur le vieillissement (CdRV). Généticien moléculaire de renommée internationale, il s'intéresse aux mécanismes qui assurent la stabilité du génome, en particulier à la biologie des télomères et de la télomérase.
Il a obtenu son doctorat à l'Université de Lausanne, en Suisse, avant d'effectuer un stage
postdoctoral au Fred Hutchinson Cancer Research Center de Seattle, sous la direction de V. A. Zakian. En 1994, il s'est joint au Département de microbiologie et d'infectiologie de la FMSS de l'Université de Sherbrooke à titre de professeur-chercheur. Il en a assumé la direction de 2008 à 2016, puis a occupé le poste de directeur adjoint scientifique du Centre de recherche sur le vieillissement (CDRV) de 2021 à 2023.
Le Pr Wellinger a également contribué à l'orientation de la recherche au Canada en siégeant à des comités consultatifs, notamment au conseil d'administration du FRQS et au comité aviseur en génétique du CIHR. De 2009 à 2023, il a été titulaire de la Chaire de recherche du Canada en biologie des télomères, un domaine dans lequel il est reconnu comme un leader mondial.
Les travaux de son équipe reposent sur une combinaison d'approches génétiques, moléculaires, biochimiques, microscopiques et de biologie cellulaire afin d'étudier la
réplication de l'ADN télomérique, ainsi que la maturation et la fonction de la télomérase. En 2024, il a été élu membre de la Société royale du Canada.