COVID-19
Sécuriser nos « maisons cellulaires »

Photo : Éloïc Colombo
Depuis le début de la crise, les médias et le public s’intéressent massivement à l’éventuel vaccin qui mettrait fin à cette pandémie mondiale inédite. Par contre, ce que peu savent, c’est que le vaccin n’est pas une option envisageable pour tous, en particulier pour les patients immunosupprimés qui ne peuvent développer leur immunité contre le virus. Cette réalité rend donc nécessaire l’exploration d’une autre voie pour contrer ce virus, celle du traitement des patients infectés. Ainsi, plusieurs chercheurs et chercheuses choisissent volontairement de ne pas prendre part à la course au vaccin et s’affairent plutôt, dans l’ombre des projecteurs, à élaborer des outils qui permettront à d’autres scientifiques de mieux tester l’efficacité d’éventuelles thérapies. C’est le cas du laboratoire de Philippe Sarret, professeur-chercheur et codirecteur à l’Institut de pharmacologie de Sherbrooke (IPS), de même que membre du Centre de recherche du CHUS (CRCHUS) qui a reçu en août dernier une subvention de 50 000$ du Conseil de recherches en sciences naturelles et en génie du Canada (CRSNG), en partenariat avec la compagnie sherbrookoise Immune Biosolutions pour le projet Development of a Cell-Based High-Throughput Functional Screening Assay to Study Host-Virus (COVID-19) Interaction. Le modèle de validation issu de ce projet pourrait permettre la progression de plusieurs recherches en lien avec la COVID-19.
L’article publié par l’IPS le 2 octobre dernier présentait les travaux de Richard Leduc (professeur-chercheur au CRCHUS et membre de l’IPS), ceux-ci ayant pour cible la sérine protéase TMPRSS2 que l’on sait être impliquée dans le processus d’entrée du virus dans la cellule humaine. De son côté, si le Pr. Philippe Sarret s’intéresse également au mécanisme d’entrée du virus de la COVID-19, son focus principal vise la validation et la quantification de l’efficacité de différentes thérapies capables de bloquer l’entrée du virus. Dans ce but, son étudiante au post-doctorat Marie-Édith Nepveu-Traversy (également détentrice d’un doctorat en virologie) a été appelée à contribuer à la création d’un modèle de validation qui pourrait être utilisé par tous les scientifiques qui s’intéressent à la première interaction du nouveau coronavirus (SARS-CoV-2) avec la cellule humaine: « Beaucoup de chercheurs choisissent de s’attaquer à cette première interaction (entre la protéine virale Spike et le récepteur ACE2 présent sur les cellules humaines). Le modèle cellulaire que nous avons développé permet ainsi d’évaluer le taux d’efficacité de toute molécule capable de bloquer l’entrée du virus dans les cellules humaines. », relate la jeune chercheuse. Le modèle élaboré par le laboratoire Sarret se veut l’optimisation d’une étude déjà documentée visant SARS-CoV (autre coronavirus existant), celle-ci ayant été publiée dans la revue scientifique Journal of visualized experiments (JOVE) en 2019.
La maison cellulaire et ses intrus
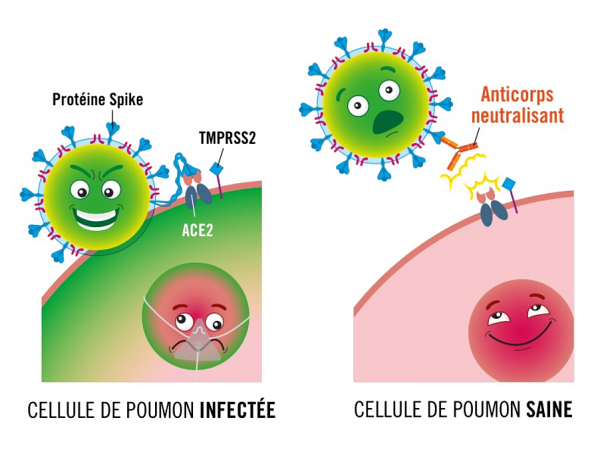
Photo : Christian Audet, graphiste
Si l’on devait illustrer le phénomène d’entrée du virus dans la cellule humaine, on pourrait le comparer au système d’entrée d’une maison. La maison (cellule humaine) présente une porte d’entrée dotée d’une serrure principale (ACE2) et d’un verrou additionnel (sérine protéase TMPRSS2). De son côté, le virus représente l’individu malveillant qui cherche par tous les moyens à pénétrer dans la maison. Comme les récentes recherches le démontrent, le virus de la COVID-19 possède la clé compatible avec la serrure principale (ACE2) à même sa propre structure (protéine Spike). Cette « clé virulante » constitue donc le point critique de l’entrée du virus dans la « maison cellulaire ». D’autre part, il a été démontré dans le cadre d’autres recherches que lorsque le verrou additionnel (TMPRSS2) n’est pas bloqué (au moyen d’une molécule inhibitrice), l’invasion du domicile s’en trouve encore plus facilitée. Le modèle développé par le laboratoire Sarret permet donc de tester différentes stratégies (molécules) de blocage visant la serrure principale, le verrou additionnel ou la clé en quantifiant de manière très précise la capacité de celles-ci à diminuer l’infection virale. Réalisables en moins de 5 jours, ces essais dits « fonctionnels » permettent de déterminer rapidement l’efficacité ou la non-efficacité de traitements potentiels.
Un intrus dangereux?
Comme il est impossible à ce stade-ci de travailler avec le « vrai » virus de la COVID-19 à moins d’avoir un niveau de confinement 3 en laboratoire, le modèle in vitro utilise un intrus que l’on appelle couramment un « pseudo-virus », celui-ci imitant le processus d’infection du SARS-CoV-2 tout en ne possédant pas le côté hautement infectieux du virus natif. Ces « pseudo-virus » COVID-19 sont composés de trois éléments : à leur surface, la protéine « Spike » du nouveau coronavirus, un environnement viral interne provenant du modèle du virus HIV (Sida) et finalement, une protéine fluorescente verte (GFP) permettant de suivre l’entrée du virus dans la cellule humaine. Une fois créés, ils peuvent entrer en interaction avec des cellules cibles qu’ils « pseudo-infectent ». La protéine fluorescente, sous une certaine lumière, permet alors d’identifier les cellules infectées et de mieux suivre l’évolution de l’infection.
S’attaquer au virus directement
Le modèle créé par le laboratoire Sarret est présentement utilisé par l’entreprise privée Immune Biosolutions dans des tests de validation de molécules de type « anticorps ». Pour le moment, celles-ci sont développées dans le but de s’attaquer directement à la clé elle-même (Spike) afin de la neutraliser. Cette stratégie, indisposant hautement l’intrus, pourrait rendre impossible le « déverouillage» de la serrure principale et donc, l’entrée du virus dans l’organisme. Toutefois, il n’est pas exclu qu’Immune Biosolutions s’intéresse également, dans un avenir rapproché, à des molécules de type « anticorps » visant le verrou ou la serrure principale de l’hôte.
Molécules inhibitrices, anticorps…tous doivent d’abord être testés afin que leur efficacité puisse être démontrée. À ce stade-ci des recherches, une question demeure : doit-on s’attaquer à l’une ou l’autre des serrures de la maison ou encore directement à l’intrus et à sa « clé virulante »? Le modèle que propose le laboratoire Sarret autorise l’exploration des trois stratégies, de même qu’une éventuelle synergie entre celles-ci qui pourrait permettre de développer une trithérapie pour une plus grande efficacité de traitement. Les chercheurs et les chercheuses poursuivent donc leur quête : quelle sera la combinaison gagnante qui sécurisera une bonne fois pour toute nos « maisons cellulaires »?
Autres publications (modèle de prolifération virale)
Collectif. Protocol and reagents for pseudotyping lentiviral particles with SARS-CoV-2 Spike protein for neutralization assays (2020). bioRxiv. Vol. 2050513. Repéré à : https://www.biorxiv.org/content/10.1101/2020.04.20.051219v1
Collectif. Optimized Pseudotyping Conditions for the SARS-COV-2 Spike Glycoprotein. (2020). Journal of virology, America Society for Microbiology. Vol.1062. Repéré à: https://jvi.asm.org/content/94/21/e01062-20